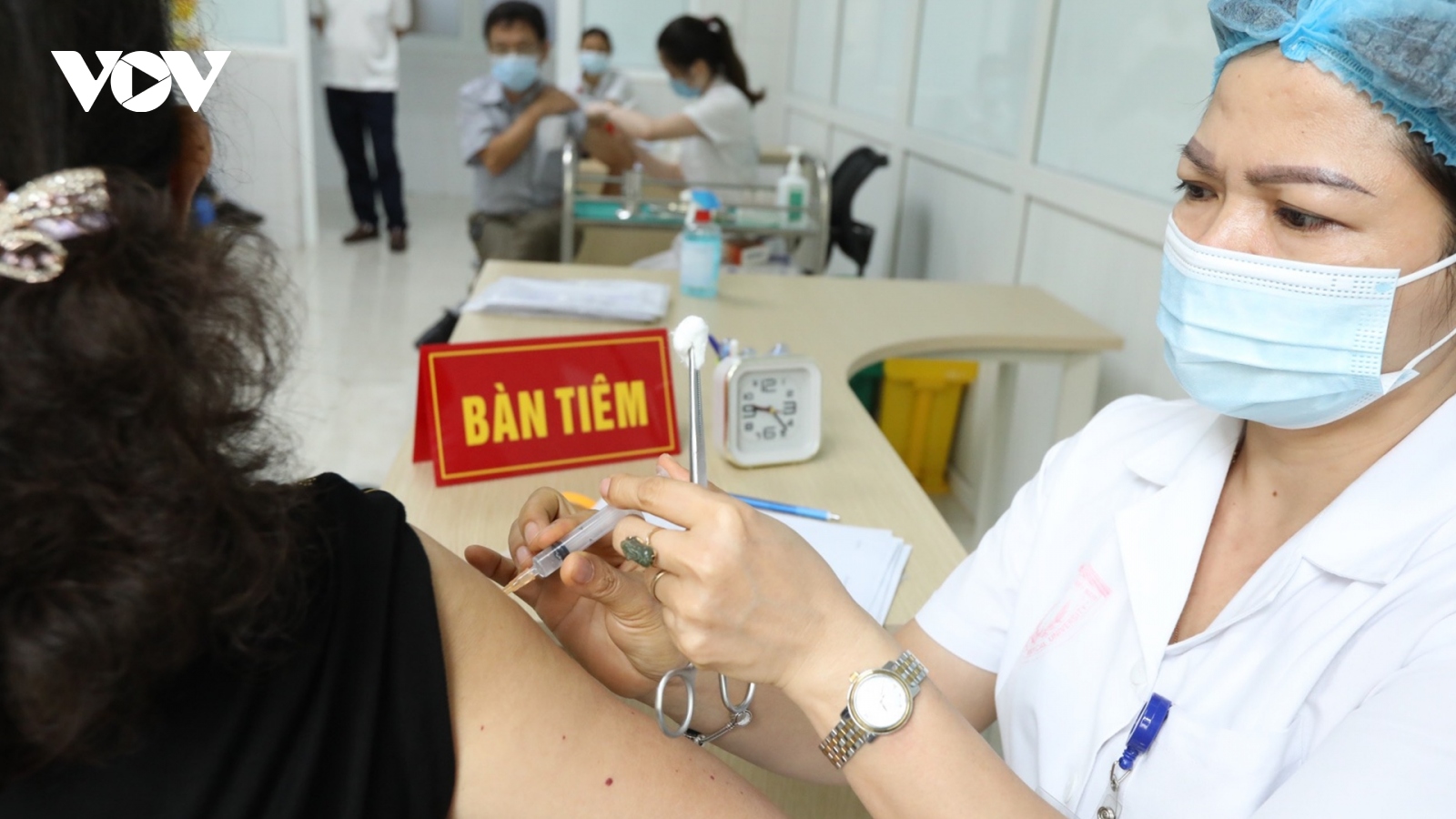
Bộ Y tế ủng hộ các tỉnh thử nghiệm lâm sàng vaccine Nano Covax nhưng cần đúng quy trình
VOV.VN - Thứ trưởng Bộ Y tế Trần Văn Thuấn cho biết, việc các tỉnh đăng ký tham gia thử nghiệm lâm sàng cần phải đúng quy trình nghiên cứu, cần thông qua Hội đồng Đạo đức, sau đó tổ chức đánh giá theo đúng các tiêu chí trong đề cương.
Trước diễn biến dịch COVID-19 phức tạp, dự báo sắp tới số ca mắc COVID-19 trên địa bàn tỉnh Bình Dương sẽ còn tăng cao, vừa qua, UBND tỉnh Bình Dương vừa có công văn hỏa tốc gửi Bộ Y tế về việc xin tham gia chương trình tiêm thí điểm vaccine Nano Covax giai đoạn 3.
Trước đó, Liên đoàn Doanh nghiệp tỉnh Bình Dương đã có văn bản gửi UBND tỉnh đề xuất đăng ký tham gia chương tình tiêm thí điểm vaccine Nano Covax giai đoạn 3 cho 200.000 tình nguyện viên là nhân viên và công nhân lao động của các hiệp hội và doanh nghiệp.
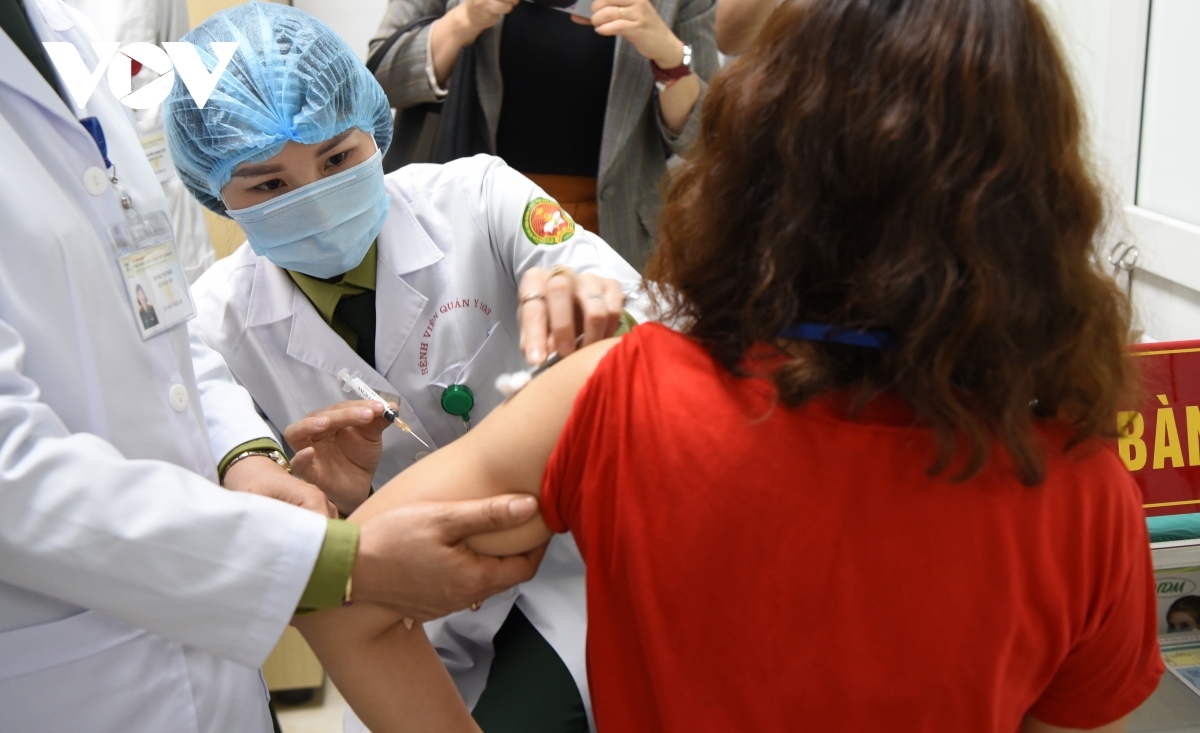
Vì vậy, UBND tỉnh Bình Dương đề nghị Bộ Y tế xem xét tạo điều kiện cho Liên đoàn Doanh nghiệp tỉnh Bình Dương được tham gia chương trình trong thời gian sớm nhất.
Ngoài Bình Dương, các tỉnh Khánh Hòa, Đồng Tháp cũng đã có văn bản gửi Bộ Y tế với mong muốn tham gia thử nghiệm đợt 3 vaccine Nano Covax.
Trước việc nhiều tỉnh xin tiêm vaccine Nano Covax, ngày 3/8, Thứ trưởng Bộ Y tế Trần Văn Thuấn cho biết, Bộ Y tế rất ủng hộ các tỉnh tham gia thử nghiệm lâm sàng vaccine Nano Covax để mở rộng phạm vi nghiên cứu nhằm đánh giá sự an toàn và hiệu quả của vaccine.
Tuy nhiên, việc đăng ký tham gia thử nghiệm lâm sàng cần phải đúng quy trình nghiên cứu, cần thông qua Hội đồng Đạo đức, sau đó tổ chức đánh giá theo đúng các tiêu chí trong đề cương.
Thứ trưởng Trần Văn Thuấn cũng cho biết, do số lượng mẫu lớn, trong quá trình thử nghiệm phải đảm bảo thu thập, quản lý dữ liệu một cách khoa học, tin cậy, chính xác và rất cần sự phối hợp của sở y tế các tỉnh.
Ông Thuấn cũng cho biết, trong tình hình hiện nay, Bộ Y tế tuyệt đối không ủng hộ việc mua bán, mượn danh thử nghiệm lâm sàng để tiêm vaccine cho người dân khi chưa được các cơ quan chức năng cấp phép.
Hiện nay Nano Covax là ứng viên vaccine ngừa COVID-19 đầu tiên của Việt Nam thử nghiệm lâm sàng pha 3a và 3b trên 13.000 tình nguyện viên. Trong đó, hơn 4.000 tình nguyện viên được tiêm đủ 2 mũi.
Ngày 2/8, Công ty Nanogen, đơn vị sản xuất cũng kiến nghị Bộ Y tế, Hội đồng Đạo đức xem xét triển khai nghiên cứu giai đoạn 3c trên 500.000-1.000.000 người.
Thứ trưởng Trần Văn Thuấn cho biết, Bộ Y tế luôn ủng hộ, mong muốn và tạo điều kiện thuận lợi nhất cho các công ty, cá nhân tham gia vào quá trình sản xuất vaccine phòng chống COVID-19 vì vậy, đã huy động nhiều nhà khoa học đầu ngành của đất nước tham gia vào đánh giá, nghiên cứu và thẩm định.
Bộ Y tế đề nghị Công ty cổ phần Công nghệ sinh học dược Nanogen, trước ngày 15/8/2021, phải gửi báo cáo dữ liệu nghiên cứu pha 2 và bước đầu pha 3, từ đó Bộ Y tế có số liệu gửi Hội đồng đạo đức và Hội đồng cấp phép của Bộ Y tế xem xét cấp phép trong tình trạng khẩn cấp./.